Nella serata del 30 dicembre sono stati pubblicati sul New England Journal of Medicine i risultati di efficacia e sicurezza derivanti dallo studio del vaccino contro il Covid-19 prodotto dall’azienda Moderna. Dopo l’approvazione del vaccino di Pfizer/BioNTech, un’altra arma si aggiunge alla lotta contro il Covid-19, che ora ha i minuti sempre più contati.
Confermata efficacia del vaccino Moderna, i risultati pubblicati su NEJM

Vaccino Moderna: confermata efficacia del 94,1% contro infezione e del 100% contro infezione severa
Per verificare l’efficacia del vaccino in esame è stato condotto uno studio di efficacia multicentrico, internazionale, controllato con placebo e in cieco per gli osservatori.
Per far ciò sono stati assegnati in modo casuale persone di età pari o superiore a 18 anni con un rapporto 1:1 per ricevere due dosi a 21 giorni di distanza di placebo o del candidato vaccino mRNA-1273.
Gli outcome primari erano due: l’efficacia del vaccino contro il Covid-19 e la sua sicurezza.
Il vaccino Moderna
Poco dopo che nel gennaio 2020 è stata determinata la sequenza genetica SARS-CoV-2, è stato sviluppato da Moderna e dal Vaccine Research Center presso il National Institute of Allergy and Infectious Diseases (NIAID) il vaccino mRNA-1273, un vaccino mRNA incapsulato con nanoparticelle lipidiche che esprime la glicoproteina spike stabilizzata in prefusione.
Questo vaccino ha dimostrato protezione negli esperimenti di provocazione sugli animali e ha mostrato in fase iniziale dati incoraggianti rispetto la sicurezza e l’immunogenicità nei test condotti sull’uomo.
Il vaccino mRNA-1273, fornito come liquido sterile a una concentrazione di 0,2 mg per millilitro, è stato somministrato mediante iniezione nel muscolo deltoide secondo un regime a due dosi. Le iniezioni sono state somministrate a 28 giorni di distanza, nello stesso braccio, in un volume di 0,5 ml contenenti 100 μg di mRNA-1273.
Il vaccino mRNA1273 è stato conservato a una temperatura compresa tra 2°C e 8° C prima della preparazione e della vaccinazione. Per questo vaccino non è stata richiesta alcuna diluizione e le dosi possono essere mantenute in siringhe fino a 8 ore a temperatura ambiente prima della somministrazione.
Caratteristiche del campione dello studio
I partecipanti idonei erano rappresentati da persone di età pari o superiore a 18 anni senza storia nota di infezione da SARS-CoV-2 e con residenza o circostanze che li esponevano a un rischio apprezzabile di infezione da SARSCoV-2 e/o ad alto rischio di contrarre una forma di Covid-19 grave.
I partecipanti sono stati assegnati in modo casuale in un rapporto 1:1, attraverso l’uso di un sistema tecnologico di risposta interattiva centralizzata, per ricevere vaccino o placebo. L’assegnazione è stata stratificata, sulla base dell’età e dei criteri di rischio per le complicanze del Covid-19, nei seguenti gruppi di rischio: persone di età pari o superiore a 65 anni, persone di età inferiore ai 65 anni che erano ad alto rischio di Covid-19 grave e persone di età inferiore ai 65 anni senza rischio elevato.
I partecipanti di età inferiore ai 65 anni sono stati classificati come soggetti a rischio di Covid-19 grave se avevano almeno uno dei seguenti fattori di rischio:
- Malattia polmonare cronica: enfisema, bronchite cronica, fibrosi polmonare idiopatica, fibrosi cistica o asma da moderata a grave
- Malattie cardiache: insufficienza cardiaca, malattia coronarica congenita, cardiomiopatie o ipertensione polmonare
- Obesità grave: BMI ≥ 40
- Diabete: tipo 1, tipo 2 o gestazionale
- Malattia del fegato
- Infezione con il virus dell’immunodeficienza umana
La preparazione e la somministrazione della dose di vaccino sono state eseguite da farmacisti e amministratori di vaccino che erano a conoscenza degli incarichi di trattamento ma non avevano altro ruolo nella conduzione dello studio.
Outcome dello studio
Sicurezza
Le valutazioni della sicurezza includevano:
- Il monitoraggio degli eventi avversi locali e sistemici avvenuti 7 giorni dopo ogni iniezione
- Le reazioni avverse avvenute 28 giorni dopo ogni iniezione
- Gli eventi avversi che hanno portato alla sospensione della somministrazione di una dose, alla partecipazione allo studio o ad entrambi
- Gli eventi avversi assistiti da un medico e gli eventi avversi gravi dal giorno 1 al giorno 759
I casi di Covid-19 e Covid-19 grave sono stati continuamente monitorati dal comitato di monitoraggio dei dati e della sicurezza dalla randomizzazione in poi.
Efficacia
Outcome primario
L’outcome primario era rappresentato dall’efficacia del vaccino mRNA-1273 nel prevenire una prima comparsa di Covid-19 sintomatico con insorgenza almeno 14 giorni dopo la seconda iniezione nella popolazione per protocollo tra i partecipanti che erano sieronegativi al basale. I casi di Covid-19 sono stati definiti se i partecipanti presentavano almeno due dei seguenti sintomi:
- Febbre (temperatura ≥38 ° C)
- Brividi
- Mialgia
- Cefalea
- Mal di gola
- Nuovi disturbi dell’olfatto o del gusto
Inoltre, i casi di Covid-19 erano confermati se i sintomi elencati si verificavano in coloro che aveva almeno un segno o sintomo respiratorio (inclusi tosse, mancanza di respiro o evidenza clinica o radiografica di polmonite) e almeno un tampone nasofaringeo, un tampone nasale o un campione di saliva (o campione respiratorio, se il partecipante era ricoverato in ospedale) che è risultato positivo per SARS-CoV-2 mediante test RT-PCR.
Tutti i partecipanti sono stati valutati per la presenza di anticorpi leganti SARS-CoV-2 specifici per la proteina nucleocapsidica SARS-CoV-2 e hanno ricevuto un tampone nasofaringeo per il test SARS-CoV-2 RT-PCR prima di ogni iniezione.
I volontari infettati da SARS-CoV-2 sono stati seguiti quotidianamente per 14 giorni o fino alla risoluzione dei sintomi per valutare la gravità dei sintomi.
La coerenza dell’efficacia del vaccino rispetto all’outcome primario è stata valutata in vari sottogruppi, inclusi i gruppi di età (da 18 a < 65 anni di età e ≥ 65 anni), l’età e il rischio per lo sviluppo di malattie gravi (da 18 a < 65 anni e non a rischio; da 18 a < 65 anni e a rischio; e ≥ 65 anni), sesso (femmina o maschio), etnia e rischio di grave malattia da Covid-19.
Outcome secondari
Il primo outcome secondario era rappresentato dall’efficacia dell’mRNA-1273 nella prevenzione del Covid-19 grave, sindrome definita dalla presenza di uno dei seguenti criteri:
- Frequenza respiratoria di 30 o più atti respiratori al minuto
- Frequenza cardiaca pari o superiore a 125 battiti al minuto
- Saturazione di ossigeno al 93% o meno in aria ambiente o un rapporto tra la pressione parziale di ossigeno e la frazione di ossigeno inspirato (P/F) inferiore a 300 mm Hg
- Insufficienza respiratoria
- Sindrome da distress respiratorio acuto
- Evidenza di shock: pressione sanguigna sistolica < 90 mm Hg, pressione sanguigna diastolica < 60 mm Hg o necessità di vasopressori
- Disfunzione renale, epatica o neurologica acuta clinicamente significativa
- Ricovero in un’unità di terapia intensiva
- Morte
Ulteriori outcome secondari includevano l’efficacia del vaccino nel prevenire il Covid-19 dopo una singola dose o nel prevenire il Covid-19 secondo una definizione di caso meno restrittiva, ovvero avere qualsiasi sintomo di Covid-19 e un test RT-PCR positivo.
Risultati
Sicurezza
Reattogenicità locale
Gli eventi avversi avvenuti nel sito di iniezione si sono verificati più frequentemente nel gruppo mRNA-1273 rispetto al gruppo placebo dopo sia la prima dose (84,2%, vs 19,8%) che la seconda dose (88,6%, vs 18,8%).
Nel gruppo mRNA-1273, gli eventi avvenuti nel sito di iniezione erano principalmente di gravità di grado 1 o 2 e sono durati in media rispettivamente 2,6 e 3,2 giorni dopo la prima e la seconda dose.
L’evento più comune nel sito di iniezione è stato il dolore dopo l’iniezione (86,0%). Si sono inoltre verificate reazioni ritardate (con insorgenza il giorno 8 o successivo) nel sito di iniezione e sono state osservate in 244 partecipanti (0,8%) dopo la prima dose e in 68 partecipanti (0,2%) dopo la seconda dose. Le reazioni erano caratterizzate da eritema, indurimento e dolorabilità e si sono risolte nei successivi 4-5 giorni.
Reattogenicità sistemica
Gli eventi avversi sistemici si sono verificati più spesso nel gruppo mRNA-1273 rispetto al gruppo placebo dopo sia la prima dose (54,9%, contro 42,2%) che la seconda dose (79,4%, contro 36,5%). La gravità degli eventi sistemici è aumentata dopo la seconda dose nel gruppo mRNA-1273, con un aumento delle proporzioni degli eventi di grado 2 (dal 16,5% dopo la prima dose al 38,1% dopo la seconda dose) e degli eventi di grado 3 (dal 2,9% al 15,8%).
Gli eventi avversi sistemici avvenuti nel gruppo mRNA-1273 sono durati una media di 2,6 giorni e 3,1 giorni rispettivamente dopo la prima e la seconda dose. Sia gli eventi avversi al sito di iniezione richiesti che quelli sistemici erano più comuni tra i partecipanti più giovani (da 18 a < 65 anni di età) rispetto ai partecipanti più anziani (≥ 65 anni di età). Inoltre, gli eventi avversi erano meno comuni nei partecipanti che erano positivi per l’infezione da SARS CoV-2 al basale rispetto a quelli che erano negativi al basale.
Si sono verificati tre decessi nel gruppo placebo (uno per perforazione intra-addominale, uno per arresto cardiorespiratorio e uno per sindrome infiammatoria sistemica grave in un partecipante con leucemia linfocitica cronica ed eruzione bollosa diffusa) e due nel gruppo vaccino (uno per arresto cardiorespiratorio e uno per suicidio).
Eventi avversi
La frequenza degli eventi avversi di grado 3 nel gruppo placebo (1,3%) è stata simile a quella nel gruppo vaccino (1,5%), così come le frequenze degli eventi avversi assistiti dal medico (9,7% contro 9,0%) e degli eventi avversi gravi (0,6% in entrambi i gruppi). Le reazioni di ipersensibilità sono state riportate nell’1,5% e nell’1,1% dei partecipanti rispettivamente ai gruppi vaccino e placebo.
La paralisi di Bell si è verificata nel gruppo vaccino (3 partecipanti, <0,1%) e nel gruppo placebo (1 partecipante, <0,1%).
Complessivamente, lo 0,5% dei partecipanti nel gruppo placebo e lo 0,3% nel gruppo mRNA-1273 ha avuto eventi avversi che hanno portato a non ricevere la seconda dose e meno dello 0,1% dei partecipanti in entrambi i gruppi ha interrotto la partecipazione allo studio a causa di eventi avversi avvenuto dopo qualsiasi dose.
Non è stata osservata alcuna evidenza di malattia respiratoria potenziata associata al vaccino e sono stati osservati meno casi di Covid-19 grave o di altre forme di Covid-19 tra i partecipanti che hanno ricevuto mRNA-1273 rispetto a quelli che hanno ricevuto placebo.
Gli eventi avversi che sono stati ritenuti dal team di studio correlati al vaccino o al placebo sono stati segnalati tra il 4,5% dei partecipanti al gruppo placebo e l’8,2% nel gruppo mRNA-1273. Gli eventi avversi correlati al trattamento più comuni (quelli riportati in almeno l’1% dei partecipanti) nel gruppo placebo e nel gruppo mRNA-1273 sono stati affaticamento (1,2% e 1,5%) e mal di testa (0,9% e 1,4%). Complessivamente, l’incidenza di eventi avversi gravi correlati al trattamento è stata maggiore nel gruppo mRNA-1273 (71 partecipanti [0,5%]) rispetto al gruppo placebo (28 partecipanti [0,2%]). L’incidenza relativa di questi eventi avversi secondo il gruppo di vaccini non è stata influenzata dall’età.
Efficacia
Dopo il giorno 1 e fino al 25 novembre 2020 sono stati identificati un totale di 269 casi di Covid-19, con un’incidenza di 79,8 casi per 1000 (IC 95% 70,5 – 89,9) tra i partecipanti al gruppo placebo senza evidenza di precedente infezione da SARS-CoV-2.
Per quanto riguarda l’analisi primaria, sono stati diagnosticati 196 casi di Covid-19: 11 casi nel gruppo vaccino (3,3 per 1000; IC 95%, 1,7 – 6,0) e 185 casi nel gruppo placebo (56,5 per 1000; IC 95% 48,7 – 65,3), indicando un’efficacia del 94,1% del vaccino mRNA-1273 (IC 95%, 89,3 – 96,8%; P <0,001) per la prevenzione dell’infezione sintomatica da SARS-CoV-2 rispetto al placebo.
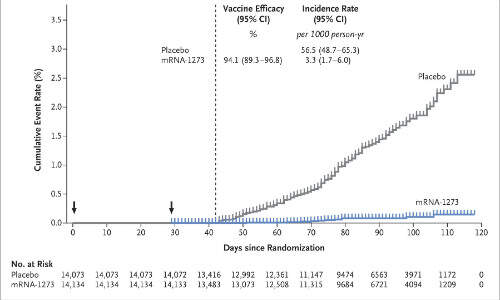
I risultati erano simili anche nelle principali analisi secondarie, inclusa la valutazione a partire da 14 giorni dopo la dose 1 (225 casi con placebo, vs 11 con mRNA-1273, indicando un’efficacia del vaccino del 95,2% [IC 95% 91,2 – 97,4]), e la valutazione che includeva i partecipanti che erano SARS-CoV-2 sieropositivi al basale (187 casi con placebo, vs 12 con mRNA1273, indicando l’efficacia del vaccino del 93,6% [IC95% 88,6 – 96,5]).
Tra i giorni 1 e 42, sono stati identificati sette casi di Covid-19 nel gruppo mRNA-1273 rispetto a 65 casi nel gruppo placebo.
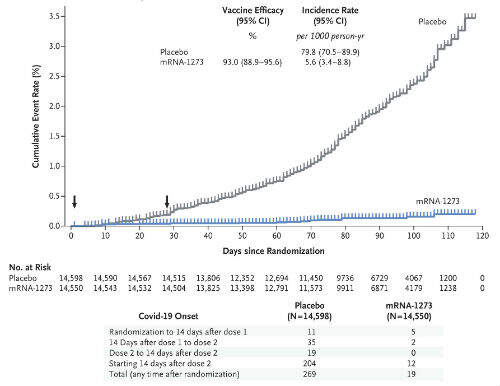
Un outcome secondario chiave ha valutato l’efficacia dell’mRNA-1273 nella prevenzione del Covid19 in forma grave. Trenta partecipanti allo studio avevano un Covid-19 grave e tutti e 30 erano nel gruppo placebo (indicando un’efficacia del vaccino del 100% e un decesso tra questi partecipanti è stato attribuito al Covid-19. L’efficacia del vaccino per prevenire il Covid-19 è risultata coerente tra i sottogruppi stratificati per caratteristiche demografiche e basali.
















Commento (0)
Devi fare il login per lasciare un commento. Non sei iscritto ?