Molte persone sostengono che il vaccino contro il Covid-19 sia stato prodotto troppo velocemente e studiato troppo poco, minando in questo modo la sua sicurezza. Ecco perché non è così.
La situazione straordinaria ha permesso di velocizzare l’intero processo
Il vaccino anti Covid Pfizer/BioNTech
In condizioni normali, lo sviluppo di un nuovo vaccino può richiedere tra i 10 e i 15 anni dall’inizio della ricerca alla sua messa in commercio. Questo ampio lasso di tempo è necessario per compiere una serie di passaggi necessari affinché la nuova vaccinazione possa essere approvata e somministrata in larga scala.
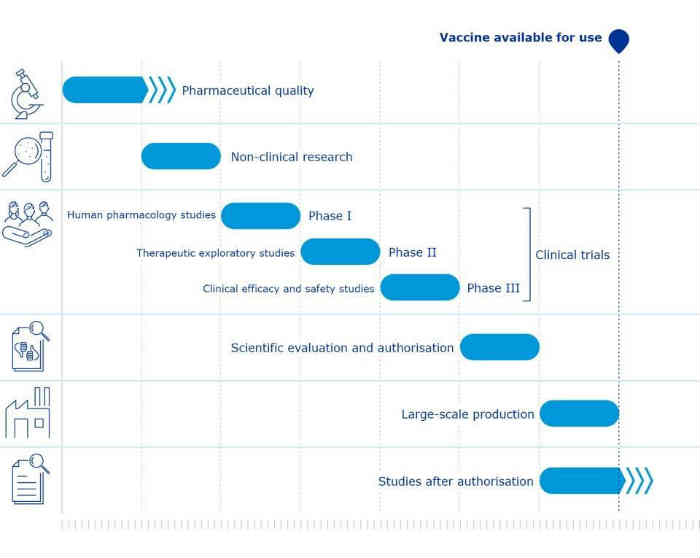
Per quanto riguarda la pandemia da Covid-19 anche in questo caso i vari test clinici sono stati condotti con lo stesso rigore e con la stessa durata. Quello che è cambiato è che sono stati accelerati i finanziamenti, la burocrazia, la ricerca di strutture e volontari e la valutazione finale.
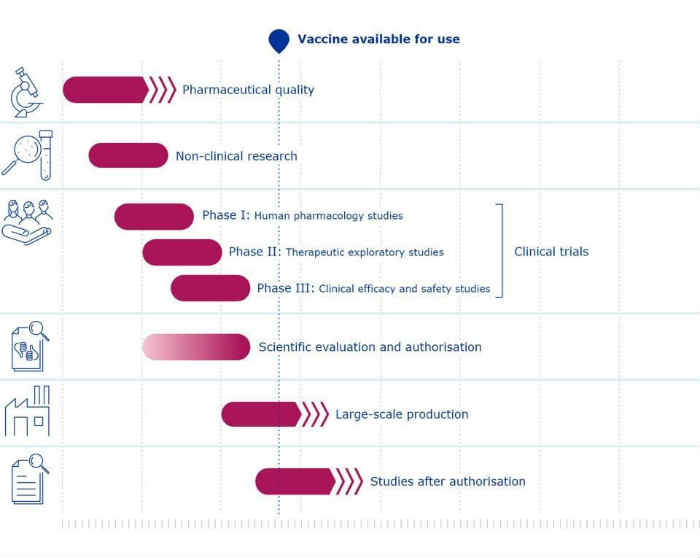
Al fine di contrastare questa pandemia le varie aziende hanno stanziato immediatamente dei fondi urgenti, abbreviando così di 1-3 anni tutto il processo che solitamente richiedeva molto tempo nelle sue fasi iniziali appunto per ricercare fondi per sostenere la ricerca stessa. Inoltre, le strutture ospedaliere e universitarie hanno sin da subito accettato di ospitare le sperimentazioni e sono stati subito trovati i volontari in un numero conforme (se non superiore) agli standard, permettendo in questo modo di risparmiare complessivamente circa 2 anni.
Per quanto riguarda la tecnologia utilizzata - il famoso mRNA - questo metodo era già noto ai ricercatori grazie agli studi condotti in precedenza su SARS e MERS. Questo fattore ha contribuito considerevolmente nell’abbreviare i tempi, permettendo ai ricercatori di accorciare questo processo di circa 5 anni. Inoltre, il fatto che questa tecnologia non debba essere studiata su colture cellulari, in quanto fase non necessaria per il Covid-19, ha abbreviato i tempi di un anno.
Fasi di sperimentazione clinica
In riferimento alle fasi di sperimentazione clinica, queste sono sempre state 3 della durata di 3-6 mesi ciascuna:
- Studio di fase I: sperimentazione clinica che prevede l'uso di un farmaco per la prima volta nell'uomo, con l’obiettivo di definirne la tossicità. Lo scopo è identificare la dose massima sicura con cui quel farmaco può essere somministrato ai pazienti senza eccessivi rischi di tossicità
- Studio di fase II: ha lo scopo di valutare l’attività del farmaco o della combinazione di farmaci contro una malattia specifica e la sua tossicità alla dose precedentemente selezionata. Una volta che i risultati dello studio di fase I hanno stabilito che un paziente può ricevere una dose di farmaco senza rischi eccessivi, si cerca di definirne l’attività contro la malattia, basandosi sull’assunto quasi sempre vero che se un farmaco tiene sotto controllo la malattia produrrà un beneficio per il paziente
- Studio di fase III: è finalizzata a valutare il beneficio per i pazienti, confrontando un gruppo di pazienti trattati con il trattamento che si è dimostrato attivo nella fase II con un altro gruppo trattato con la terapia standard per la patologia su cui si sta lavorando, cioè quella già adottata dalla comunità scientifica come la migliore a disposizione
Per quanto riguarda il vaccino contro il Covid-19, queste tre fasi sono state condotte praticamente in contemporanea tra loro, col rischio che una problematica emersa in una fase avrebbe portato all’annullamento dell’intera sperimentazione. Tuttavia, queste problematiche non sono emerse e quest’accelerazione ha portato al risparmio di 6 mesi.
Infine, al termine di queste tre fasi, le autorità competenti hanno valutato immediatamente i dati forniti dalle aziende farmaceutiche, dedicandone moltissimi revisori.
In questo modo, i vaccini contro il Covid-19 sviluppati in quest’anno hanno avuto la precedenza e la priorità assoluta rispetto ad altri farmaci in attesa di sperimentazione, facendo sì che i vari comitati di approvazione si riunissero addirittura in sessioni straordinarie pochi giorni dopo il ricevimento dei dati di sicurezza ed efficacia. Questo passaggio ha fatto sì che l’intero processo fosse abbreviato di ulteriori 3-4 anni.
















Commento (0)
Devi fare il login per lasciare un commento. Non sei iscritto ?